BLOKÁTORY PUBERTY U DĚTÍ: VAROVÁNÍ PŘED TRVALÝMI NÁSLEDKY
Tisíce hlášení pro americkou FDA o nežádoucích účincích blokátorů puberty
Podle dostupných svědectví a hlášení nežádoucích účinků se kolem léku Lupron, využívaného k potlačení puberty, hromadí vážné otázky. Některé osoby popisují dlouhodobé bolesti, řídnutí kostí, psychické potíže a další stavy, které se běžně objevují až ve vyšším věku.
FDA provádí specifický přezkum neurologických a psychiatrických příhod
Americká FDA přitom uvádí, že provádí specifický přezkum neurologických a psychiatrických příhod u pediatrických pacientů, a zároveň řeší i hlášení smrtelných záchvatů spojených s pediatrickým užitím léků ze skupiny agonistů GnRH, jak informuje server kffhealthnews.org.
Příběh Sharissy a společný jmenovatel „Lupron“
Po celá léta neměla Sharissa Derricottová (30) tušení, proč její tělo selhává. Ve 21 letech jí chirurg vyměnil poškozený čelistní kloub, byla jí diagnostikována degenerativní onemocnění meziobratlových plotének a fibromyalgie a zuby jí ztrácejí sklovinu a praskají.
Zlom nastal až ve chvíli, kdy narazila na online komunitu žen s podobnými příznaky a jednou společnou zkušeností: všechny užívaly lék zvaný Lupron. Derricottová z Lawtonu v Oklahomě to shrnula takto: „Mám pocit, jako bych byl trestán za to, že na mně v dětství prováděli pokusy,“ a dodala: „Nerad bych, aby dítěti předepsali Lupron, aby se dostalo do mého věku a prošlo si tím, čím jsem prošel já.“
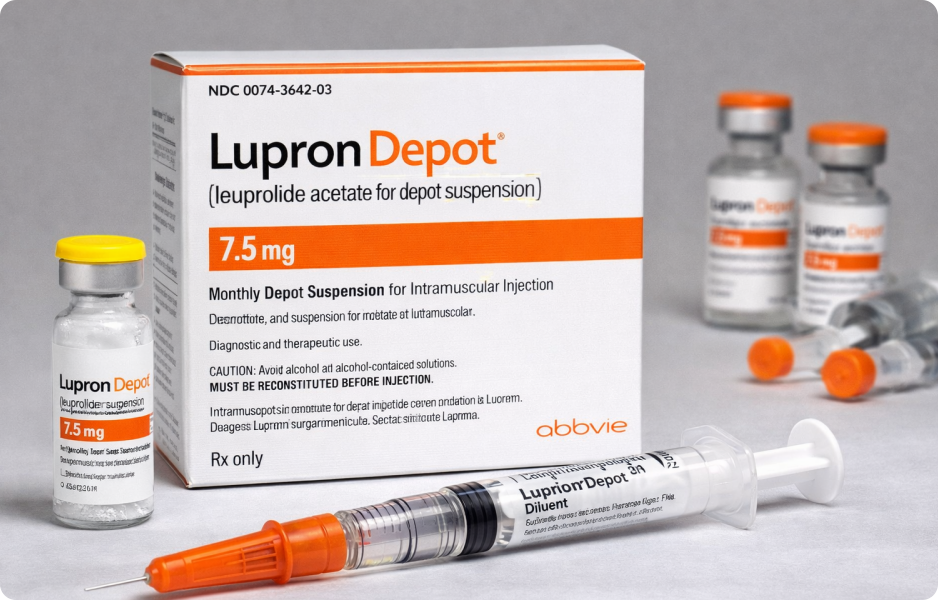
Co je Lupron a proč se podává dětem
Tisíce rodičů se rozhodly podávat tento lék dcerám, protože byl schválen k potlačení puberty u mladých dívek. Zároveň se ale používá i mimo schválené indikace, například s cílem podpořit růst u dětí menšího vzrůstu.
Pediatrická verze obsahuje varování ohledně dlouhodobých vedlejších účinků. U dospělých se Lupron používá například při léčbě rakoviny prostaty nebo k úlevě od bolesti dělohy a FDA uvádí na etiketách pro dospělé varování před různými vedlejšími účinky.
Desítky tisíc hlášení a typické potíže, které se opakují
Více než 10 000 hlášení nežádoucích účinků podaných FDA odráží zkušenosti osob, které Lupron užívaly. Hlášení popisují vše od křehkých kostí až po poruchy kloubů.
V rozhovorech a na internetových fórech se objevují popisy závažných vedlejších účinků, které jsou u dospělých dobře zdokumentovány. Zmiňují se nejen krátkodobé projevy uvedené na pediatrickém štítku (bolest v místě vpichu, výkyvy nálady, bolesti hlavy), ale i stavy typické spíše pro pozdější věk: dvacetiletá osoba z Jižní Karolíny s osteopenií, pětadvacetiletá osoba z Pensylvánie s osteoporózou a zlomeninou páteře, šestadvacetiletá osoba z Massachusetts s nutností totální náhrady kyčelního kloubu či pětadvacetiletá osoba z Wisconsinu s chronickými bolestmi a degenerativním onemocněním meziobratlových plotének.
FDA prověřuje neurologické a psychiatrické příhody
Část stížností se týká depresí, úzkostí a u některých případů i sebevražedných sklonů. Objevují se také popisy záchvatů.
FDA k tomu ve svém prohlášení uvedla: „V současné době provádíme specifický přezkum nervového systému a psychiatrických příhod souvisejících s užíváním agonistů GnRH [třídy léků], včetně Lupronu, u pediatrických pacientů,“ a současně prověřuje i smrtelné záchvaty související s pediatrickým použitím Lupronu a dalších léků této třídy. Zároveň však dosud nevydala další varování týkající se použití u dětí a neschválené používání přetrvává.
Off-label předepisování: v USA legální, ale s nejasným rizikem
Vedle zdravotních hlášení se kritika zaměřuje i na praxi „off-label“ předepisování, tedy použití způsobem, který FDA neposoudila jako bezpečný a účinný. V textu se uvádí, že někteří odborníci kritizují využívání Lupronu k tomu, aby děti s normálním časováním puberty vyrostly do větší výšky, a že škody takové praxe byly prokázány už před více než deseti lety.
V roce 2009 mezinárodní konsorcium pediatrů před podobným používáním varovalo. Mezi nimi byla i pediatrická endokrinoložka Dr. Erica Eugster, jejíž výzkum upozornil, že léky oddalující pubertu jsou široce používány mimo indikace, aniž je bezpečnost takového postupu prokázána.
Otázky bez jasné odpovědi: „Nikdo z nás na to nedokáže odpovědět.“
Zdravotní problémy popsané více než tuctem žen v rozhovorech mají podle textu ilustrovat možné dlouhodobé účinky pediatrického použití a vyžadují další vyšetřování.
Dr. Alan Rogol, emeritní profesor pediatrie na Lékařské fakultě Univerzity Virginie, který uvedl, že tento lék předepisoval po celá desetiletí, to komentoval slovy: „To je otázka, kterou si musíte položit: ‚Je to příliv?‘“ a dodal: „Nikdo z nás na to nedokáže odpovědět.“
Schválení a sporné podklady z roku 1993
Výrobce AbbVie uvádí, že studie bezpečnosti byly předloženy FDA před schválením pediatrického použití v roce 1993 pro léčbu centrální předčasné puberty. Příbalová informace tento stav definuje jako nástup pohlavních znaků před 8. rokem u dívek a před 9. rokem u chlapců. Mluvčí Morry Smulevitz k tomu napsal: „Použití nad rámec schváleného označení na etiketě se považuje za neschválené použití.“
Federální záznamy však popisují i vnitřní výhrady. V dopise z roku 1993 získaném na základě zákona o svobodném přístupu k informacím bývalý úředník FDA Dr. Alexander Fleming napsal, že je „politováníhodné“, že komise schválila léčivo po minimálním posouzení. Uvedl, že jedna studie sledovala 22 dětí pouze šest měsíců a druhou studii popsal jako „volnou“ revizi, která ztěžovala určení optimální dávky. Přesto podpořil schválení „vzhledem k absenci lepšího přístupu“.
Studie z roku 2010 a „záhadné“ opomenutí vedlejších účinků
Další studie sponzorovaná výrobcem, dokončená dlouho po Flemingově dopise, sledovala děti užívající Lupron na předčasnou pubertu v letech 1991 až 2009. Zpráva z roku 2010 předložená FDA uváděla, že sedm z 55 dětí trpělo závažnými vedlejšími účinky, ale tvrdila, že se Lupron mohl týkat jen některých z nich.
Podle databáze klinických výzkumů Národního institutu zdraví však existují dva závažné vedlejší účinky (porucha kostí a zlomenina způsobená onemocněním), které ve studii z roku 2010 zmíněny nejsou. Dr. Ned Feder z projektu Project on Government Oversight to označil za „záhadné“ a uvedl: „Mně se to rozhodně jeví jako důvod ke kritice,“ a také: „Co to dělají? Je to náhoda?“
Peníze, přednášky a trh s Lupronem
Text popisuje i finanční souvislosti: AbbVie zaplatila autorovi studie Dr. Peteru A. Leemu v letech 2013 až 2015 částku 157 066 dolarů za cestování a přednášky o přípravku Lupron, podle veřejně dostupných údajů Medicare. Současně se uvádí, že podnikání s Lupronem bylo v roce 2013 převedeno na AbbVie a že v roce 2015 vykázala firma tržby 826 milionů dolarů.
Mluvčí Smulevitz k bezpečnosti uvedl, že AbbVie „pravidelně sleduje a předává FDA (stejně jako dalším regulačním orgánům) nové informace o bezpečnosti, aby zajistila, že naše příbalové informace obsahují přesné a aktuální informace, které pomáhají předepisujícím lékařům a pacientům“.
Derricottová: užívání od pěti do dvanácti let a „je to peklo“
Derricottová uvádí, že Lupron užívala od 5 do 12 let kvůli předčasné pubertě, a patří tak mezi první pediatrické pacienty — ještě před schválením pro pediatrické použití. Dnes říká, že podstoupila více operací než její 79letý otec a trpí poruchou krve i problémy s kostmi a klouby.
Její věta je v textu uvedena bez obalu: „Omluvte můj jazyk, ale je to peklo,“ řekla.
Historie léku: od „zázraku“ v osmdesátých letech po dlouhé kontroly
Když byly v 80. letech objeveny léky jako Lupron, byl to pro část oboru „zázrak“. Pomáhal řešit vzácné, ale znepokojivé případy, kdy se u velmi malých dětí objevovaly znaky puberty. Mechanismus je popsaný tak, že lék v mozku zastavuje tok estrogenu, a tím „zastavuje“ postup těla k pubertě; po ukončení injekcí se puberta obnoví.
Lupron byl původně schválen v roce 1989 pro léčbu rakoviny prostaty. U mužů příbalové informace varují před zvýšeným rizikem infarktu, mrtvice a náhlé smrti. Text také uvádí, že chlapci tvoří asi 10 procent dětí užívajících Lupron, často kvůli nádorům či jiným onemocněním spojeným s předčasnou pubertou.
Dvacet tisíc hlášení, devět set u dětí mladších třinácti let
Za poslední desetiletí bylo FDA nahlášeno více než 20 000 nežádoucích účinků. Zmiňují se stovky případů nespavosti, deprese a bolesti kloubů, více než 100 případů rozmazaného vidění a přibližně 900 hlášení nežádoucích účinků u dětí mladších 13 let, často během několika měsíců po užití.
FDA podle textu v roce 1999 prošetřila 6 000 hlášení, přičemž soudní dokument shrnující závěry uváděl „vysokou prevalenci závažných nežádoucích účinků“, včetně deprese, bolesti kloubů a slabosti. Text dodává, že FDA zásadní změny neprovedla, ale přezkoumala příbalové informace.
Skandál s marketingem a rekordní pokuta 875 milionů dolarů
O dva roky později se Lupron dostal na titulní stránky: ministerstvo spravedlnosti oznámilo civilní a trestní dohodu s tehdejším výrobcem. Prokurátoři uvedli, že prodejní tým odměňoval předepisující lékaře lyžařskými a golfovými výlety a úplatky. V soudním dokumentu jeden gynekolog uvedl, že mu obchodní zástupce řekl, že „může vydělat 100 000 dolarů ročně“, pokud bude léčit ženy ve své ordinaci přípravkem Lupron.
Dohoda vedla k přiznání viny za spiknutí a k pokutě 875 milionů dolarů, jedné z nejvyšších té doby.
Případ Kleinové a tvrzení o „nevratných vedlejších účincích“
V roce 2008 se Lupron znovu objevil u soudu v případu pacientky Karin Klein. Znalec Dr. John Gueriguian, bývalý lékař FDA, ve zprávě uvedl, že lék způsobuje „nevratné vedlejší účinky a trvalé vážné zdravotní problémy“.
Gueriguian také napsal: „Pokud rizika léku převyšují jeho přínosy, měl by být tento lék zakázán a stažen z trhu,“ a při pozdějším kontaktu uvedl, že nemá další komentáře. Kleinová spor prohrála a odvolání bylo zamítnuto až u Nejvyššího soudu.
Růst za cenu zdraví: náklady 20 000 až 40 000 dolarů a tisíce receptů
Text přináší i konkrétní příběh spojený s růstem. Brooklyn Harbinová uvedla, že Lupron dostala poté, co jí v 10 letech začala menstruace, a doufala v několik centimetrů navíc. Přestože výzkumy opakovaně varovaly před takovým použitím mimo indikace, v roce 2006 začala dostávat injekce.
Dr. Eugster v roce 2015 uvedl, že léčba oddalující pubertu je drahá — 20 000 až 40 000 dolarů za dvouletou léčbu. Ve studii z roku 2015 zhodnotil záznamy 260 dětí a uvedl, že 27 procent nesplňovalo definici centrální předčasné puberty; více než polovině byl lék předepsán mimo indikace s cílem zvýšit výšku. Dokumenty FDA uvádějí přibližně 2 000 případů předčasné puberty ročně, ale IMS Health hlásí, že v roce 2015 bylo vystaveno 24 000 receptů, s průměrnou cenou 8 300 dolarů za tříměsíční dávku dlouhodobě působícího přípravku.
Harbinová: kolaps po desáté injekci a „sebevražda se stala reálnou“
Harbinová popisuje kolaps po desáté injekci ve věku 10 let během nákupů ve Wal-Martu: necítila nic od kolen dolů a strávila šest měsíců na vozíku. Kvůli nízké hustotě kostí se musela vzdát sportů a v sedmé třídě strávila měsíc v Mayo Clinic v Minnesotě, kde se učila zvládat chronickou bolest.
V textu zaznívá její silná výpověď: „Měla jsem pocit, jako by mi někdo vzal malé kousky mého života a nikdo se k tomu nechtěl přiznat,“ a také: „Sebevražda se pro mě stala velmi, velmi reálnou.“
„Jako rodič se za to nenávidím… Co jsem si to jen myslel?“
Do článku vstupuje i hlas rodičů. Jeanne Walshová z Temeculy v Kalifornii říká: „Jako rodič se za to nenávidím,“ a pokračuje: „Co jsem si to jen myslela?“ Text uvádí, že Walshová dcera užívala Lupron kvůli předčasné pubertě a dnes trpí fibromyalgií a podstoupila operaci čelistního kloubu.
Dr. Eugster v této souvislosti napsal, že příliš mnoho lékařů má při obavách rodičů sklon „něco udělat“, i když bezpečnost off-label předepisování „nelze předpokládat“.
Co říkají studie o kostech: návrat k normálu, nebo trvalé škody?
Kosti a jejich hustota se v textu opakují jako klíčové téma. Studie z roku 2003 v New England Journal of Medicine dospěla k závěru, že u části dětí došlo během tříleté léčby k osteopenii a přílišnému úbytku kostní hustoty, takže celoživotní riziko zlomenin převážilo přínos mírně vyššího vzrůstu.
Jiné práce ukazují odlišný obraz. Italská studie z roku 2009 u 66 dívek uvádí nižší hustotu po léčbě, ale návrat na srovnatelnou úroveň během asi 10 let. Německá studie uvádí, že k poškození kostí nedochází, i když sedm ze 41 osob (17 procent) mělo několik let po ukončení léčby osteopenii. Na Tchaj-wanu u 11 dívek léčených zhruba od 8 let po dobu asi 5 let zjistili ve věku kolem 20 let osteopenii u 45 procent. Turecká práce uvádí nepříznivý vliv na zdraví kostí v souvislosti se závažným nedostatkem vitamínu D (13 dětí proti dvěma v kontrolní skupině). Kanadská studie z roku 2013 popisuje pět dětí s posunem dlouhé kosti nohy u kyčle kvůli „nedostatečné expozici pohlavním hormonům v ‚kritickém období‘ tvorby kostí“.
FDA: účinky na hustotu kostí u dětí jsou „neznámé“
FDA podle citovaného prohlášení považuje vliv na kosti u dětí za nezodpovězenou otázku: „Účinky na hustotu kostí u dětí, u nichž je centrální předčasná puberta zastavena agonistou GnRH, jsou považovány za ‚neznámé‘, protože nebyly studovány.“
E. Kirk Neely, profesor Stanfordovy univerzity a pediatrický endokrinolog, k dlouhodobému sledování uvedl: „Mám obavy. Je tu velmi zásadní problém. Léčíme tyto děti, ony zmizí a už je nikdy nevidíme,“ a dodal: „Nemáme dobré možnosti sledování, zejména v USA.“ Zda Lupron způsobuje dlouhodobé problémy, uzavírá citací: „odpověď zní: nevím“.
Život s bolestí, depresemi a zlomeninami: Wardová a další svědectví
Valerie Wardová (25) uvádí, že užívala Lupron od 9 do 12 let kvůli předčasné pubertě a dnes řeší nesnesitelné bolesti svalů a kostí, depresi, slabost a únavu. Ve věku 25 let prodělala záchvat, který vedl ke zlomenině obratle, a následně přišla diagnóza osteoporózy.
Wardová k bolesti řekla: „Byla to nejintenzivnější bolest, jakou jsem v životě zažil,“ stojí v textu. V další části se připomíná, že u dospělých se v příbalové informaci varuje před dlouhodobým podáváním kvůli úbytku kostní hustoty, a studie z roku 2005 u mužů s rakovinou prostaty uvádí, že Lupron „významně zvyšuje“ riziko zlomenin.
Mitochondrie jako možný klíč: „Je to řetězová reakce“
Text přináší i hypotézu o mechanismu potíží. Výzkumnice Chandler Marrsová, endokrinoložka zaměřená na zdraví žen, uvedla, že ji překvapila závažnost a délka vedlejších účinků, a proto spustila průzkum. Získala více než 1 000 dotazníků.
Osoby uváděly různé příznaky: 30 procent silné bolesti kloubů, 29 procent silné bolesti těla, 26 procent praskání zubů, 20 procent osteoporózu. Více než polovina uváděla středně těžkou až život ohrožující depresi a 15 procent hodnotilo sebevražedné myšlenky jako život ohrožující až silné.
Marrsová popisuje jednotící faktor přes estradiol a mitochondrie a uzavírá citací: „Pokud dojde k poškození mitochondrií, začnou selhávat nervy; pokud začnou selhávat nervy, selžou svaly. Je to řetězová reakce,“ řekl Marrs, výkonný ředitel výzkumné společnosti Lucine Health Sciences se sídlem v Nevadě.
















Zanechte komentář :